Reconocimiento Molecular y Organocatálisis: Mimetizando las enzimas
Receptores Quirales de Cationes
Las interacciones no-covalentes son responsables de una gran parte de las funciones de los sistemas biológicos: reconocimiento molecular, transporte, catálisis, etc. Por lo tanto, el entendimiento de las mismas es fundamental para modular las propiedades funcionales de las moléculas y de los nuevos materiales. Hemos utilizado receptores quirales de cationes como modelos sencillos para poder cuantificar alguna de estas interacciones y la forma en que estas cooperan entre sí.
Síntesis de Péptido-Miméticos y Organocatálisis
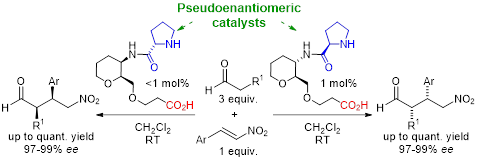
Otro de los modelos elegidos para el estudio de las interacciones no-covalentes son los péptidos miméticos cuyo objetivo es imitar la estructura peptídica disponiendo espacialmente los grupos funcionales de forma controlada. Al poseer características semejantes a sus homólogos naturales, se han utilizado para reemplazar a las enzimas o proteínas, o para interrumpir las interacciones entre proteínas. Nosotros hemos utilizados los azúcares-aminoácidos (SAA) como unidad estructural para la construcción de péptido-miméticos. Estas unidades contienen el esqueleto de un azúcar, y a su vez poseen un grupo amino y otro ácido. Estudiando los péptidos cíclicos provenientes de los ε-SAA, encontramos que pequeños cambios en el esqueleto del ε-SAA modifican de forma notable la disposición espacial de los macrociclos, debido a que se transforma el patrón de las interacciones no-covalentes intramoleculares. Trasladando este conocimiento a la organocatálisis hemos diseñado dos catalizadores pseudoenantiomericos capaces de catalizar adiciones de Michael de aldehídos a β-nitroestirenos de forma enantioselectiva utilizando cargas catalíticas menores del 1 mol %, con rendimientos prácticamente cuantitativos y excesos enantioméricos superiores al 97 %.
Tomás Martín Ruíz
